- アトピー性皮膚炎とはどんな病気?
- アトピー性皮膚炎の発症の病因とは?
- アトピー性皮膚炎の症状と経過について
- アトピー性皮膚炎の検査について
- アトピー性皮膚炎の治療について
- アトピー性皮膚炎の治療の進展と変遷
- 当院における治療について
アトピー性皮膚炎とは皮膚表面の角質層の異常にともなって、皮膚の乾燥とバリア機能異常という皮膚の生理学的異常があるために、色々な物質に対して多彩な非特異的な刺激反応や特異的なアレルギー反応が起こることによって、慢性に経過する炎症とかゆみをともなう湿疹・皮膚炎群の一疾患です。
ここで、日本皮膚科学会の定める「アトピー性皮膚炎ガイドライン」におけるアトピー性皮膚炎の定義を見てみましょう。
アトピー性皮膚炎の定義(概念)
アトピー性皮膚炎は、増悪・寛解を繰り返す、瘙痒のある湿疹を主病変とする疾患であり、患者の多くはアトピー素因を持つ。
アトピー素因:以下の①または②を満たす
①家族歴・既往歴(気管支喘息、アレルギー性鼻炎・結膜炎、アトピー性皮膚炎
のうちいずれか、あるいは複数の疾患)
②IgE抗体を産生し易い素因
このままだと少しわかりにくいかと思いますので、もう少し簡単に言い換えると次のようになります。
アトピー性皮膚炎は、かゆみのある湿疹がでる病気で、悪くなったり良くなったりを繰り返します。患者さんの多くは「アトピー素因」と呼ばれる次のような傾向をもっています。
①自分や血のつながっている親族(両親、兄弟、祖父母)がアトピー性皮膚炎や、他のアレルギー疾患(気管支喘息、アレルギー性鼻炎・結膜炎)をもっていたり、その既往がある。
②様々な物質に対して、IgE抗体と言われる即時型アレルギーに関係する抗体を産生しやすい。
正確なアトピー性皮膚炎の診断基準は、さらに詳細に年齢別に皮膚症状の特徴と分布する範囲や、症状の持続する期間をもとに定められています。
表1の「アトピー性皮膚炎の定義・診断基準」をご参照ください。
いまだにアトピー性皮膚炎の発症メカニズムは十分には解明されていませんが、まずは近年定着してきた「アトピー性皮膚炎の三位一体病態論」を紹介します。

上図のように、アトピー性皮膚炎は、①、②、③の要因が互いに関連し合って病態を形成するという考え方です。
実際の皮膚の内部では複雑な反応が起こっていますが、ここでは要点を絞って説明します。
①皮膚の生理機能異常
アトピー性皮膚炎特有の皮膚異常として、バリア機能の低下(水分保持能の低下、微生物に対する易感染性)や、発汗異常、皮膚血管反応の異常などがみられます。
角質層のバリア機能形成に重要な働きをもつ物質としてフィラグリンという蛋白質があります。フィラグリンは分解されてアミノ酸などの天然保湿因子と言われる皮膚の保水、紫外線吸収などを行う物質になる他、皮膚表面のpH(弱酸性)の維持にも重要であり、外界の微生 物からの防御にも役立っています。
アトピー性皮膚炎患者の約30%にフィラグリンをコードする遺伝子に変異がみられることが報告されており、また②で述べるType2サイトカインには皮膚の表皮層の様々な障害やかゆみを誘導する作用があり、これらによって、バリア機能低下をはじめとしたアトピー性皮膚炎特有の皮膚症状が引き起こされると考えられます。

②免疫学的要因
①の皮膚のバリア機能異常に伴って、皮膚の免疫学的異常が誘導されます。特にアトピー性 皮膚炎において主体となるのはTh2(2型ヘルパーT細胞)やILC2(2型自然リンパ球)と呼ばれるリンパ球の活性化です。
リンパ球の一種であるヘルパーT細胞(Th)には代表的なものとして、タイプ1(Th1)とタイプ2(Th2)があり、いずれも獲得免疫反応に関わる重要な細胞です。
通常はバランスをとりあって相互作用していますが、アトピー性皮膚炎や他のアレルギー疾患ではTh2細胞による反応が亢進しており、Th2細胞が優位になっています。
また、自然リンパ球(ILC)はTh細胞とは異なり、抗原の認識なしに活性化する自然免疫系の細胞であり、近年研究が進んでいる新しい細胞です。グループ1~3に分類されますが、 グループ2のILC2細胞はアトピー性皮膚炎を含むアレルギー性疾患に深く関わっています。
ここで、現在判明してるアトピー性皮膚炎の病態生理の模式図を掲載します。

上図の中心となっているTh2細胞やILC2細胞が産生する炎症性サイトカイン(Type2サイトカイン)がアトピー性皮膚炎の病変皮膚の炎症形成に深く関わっており、以下の表のようなものが知られていますが、IL(インターロイキン)と呼ばれる一群の仲間であるIL-4、IL-5、 IL-13、IL-31などが特に重要となります。
これらによって、さらなるTh2細胞の活性化や、表皮角化細胞の障害、バリア機能の低下、 抗菌ペプチド産生低下、かゆみの惹起などが引き起こされ、アトピー性皮膚炎の病態を形成します。

次の段階として、これらの炎症性サイトカインが作用するためには、標的となる細胞にその情報を伝える必要がありますが、その経路として重要なものが「JAK/STAT(ジャック・スタット)シグナル伝達経路」です。
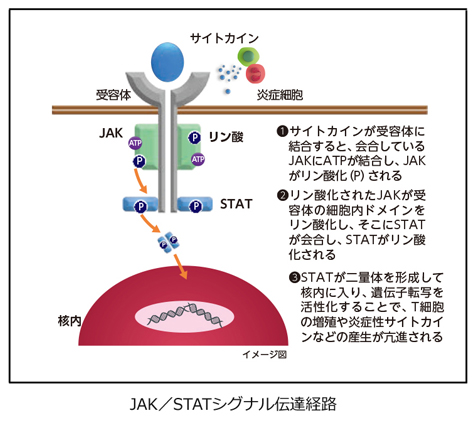
■JAK/STATシグナル伝達経路
IL-4やIL-13などの炎症性サイトカインが標的細胞の細胞膜にある受容体に結合した後、その情報が細胞内の核内にある遺伝子に伝えられるまでの主要なシグナル伝達経路です。
JAK(ヤヌスキナーゼ)はチロシンキナーゼと呼ばれる蛋白質のグループで、JAK1~3とTyk2の4種類存在します。JAKはペアを組んで細胞内側から受容体に会合していますが、 受容体にサイトカインが結合すると一方がリン酸化され活性型となり、受容体の細胞内ドメインをリン酸化します。
ここにSTATと呼ばれる蛋白質が結合してリン酸化され活性型となり、2分子のSTATが会合 して二量体を形成します。二量体となったSTATが核内に移動して、サイトカインに関連する 遺伝子群の転写が行われます。
③かゆみ、掻痒
「かゆみ」はアトピー性皮膚炎の患者様が自覚する最もつらい症状の1つであり、病態形成にも深く関わる重要な因子です。
かゆみのために皮膚をひっかくと、さらにかゆみが増強し、ひっかくことで皮膚が傷ついて さらなるバリア障害を生じて、それが炎症やかゆみを引き起こすという悪循環に陥ります。
この負のサイクルである悪循環は、「Itch-scratch サイクル」と呼ばれ、アトピー性皮膚炎の症状が長引いて、増悪する原因となります。
かゆみについては、主にType2サイトカインのIL-4やIL-31が関係してきますが、特にIL-31はかゆみを伝える末梢神経に作用してかゆみを発生させるだけでなく、末梢神経を表皮まで伸長させてかゆみに対する閾値を下げることで、かゆみ過敏状態にさせる作用もあります。
まず、アトピー性皮膚炎の症状ですが基本的には湿疹なので、「皮膚が赤くなる、細かいぶつぶつができる、じくじくする、かさかさする、ぽろぽろはがれる、かたくなる」などで、いずれも強いかゆみを伴います。
また、症状は体の左右で同じように現れやすく、おでこ、目の周り、口の周り、首、手足の関節、胸や背中などに現れます。このような症状が一時的なものではなく、長期間(ガイドラインでは乳児では2ヵ月以上、その他では6ヵ月以上)続く場合にアトピー性皮膚炎と診断されます。
また、年齢によって症状に特徴があり、一般的には乳幼児期(4歳まで)、小児期(思春期まで)、成人期(思春期以降)に分けられます。
- 乳幼児期
- 症状が顔や頭に現れやすく、かゆみの強い湿疹が生じ、細かいぶつぶつができて盛り上がったり、じくじくと液がしみ出してきたりします。
- 小児期
- 症状がひじの内側やひざの裏側などに現れるようになります。皮膚は乾燥してかさかさと皮がむけ、かゆみを伴います。耳切れもよくみられます。
- 成人期
- 広範囲にわたって顔面や上半身に治りにくい湿疹がみられ、皮膚の乾燥が強くなり、ごわごわと厚くなります。長期間湿疹が続くことで、色素沈着がみられることがあります。
次にアトピー性皮膚炎の経過ですが、一般的には年齢とともに軽快していくと考えられます。経過としては次の4パターンが考えられます。
自然寛解(症状が落ち着いて安定した状態)に関しては2、3歳頃からみられ、8~9歳頃で50%、16歳には全体の約90%が自然寛解したとの報告もありますが、アトピー性皮膚炎の予後に関する調査は少なく、明確には不明です。
アトピー性皮膚炎の年代別の有病率については報告があり、以下のグラフのようになります。年代が上がるにつれて有病率は減少しており、やはり年齢とともに寛解していく可能性が高いと考えられます。ただし、重症の割合は年齢が高いほど増える傾向があり、結局軽快に至らなかったものがそのまま成人になって重症例として残っていることが考えられます。
また近年は、思春期・成人期になっても軽快しない例や、成人発症例が増加していることが報告されています。
アトピー性皮膚炎の検査について
皮疹の状態をみるだけでも、ある程度病勢や重症度は判断することはできますが、症状を客観的に評価したり、今後の治療の目標を立てるために血液検査を行うことがあります。
アトピー性皮膚炎で高値となりやすいマーカーとして、IgE、好酸球数、LDH、TARCなどが挙げられますが、ここではTARCとIgEについて取り上げたいと思います。
TARC
TARC(thymus and activation-regulated chemokine)とはケモカインと呼ばれる白血球走化因子の一種であり、アトピー性皮膚炎では皮膚表面の様々な刺激によって角化細胞から産生され、Th2リンパ球を皮膚病変部に呼び寄せることで炎症を増悪させます。皮膚の炎症の重症度に相関して血清中のTARC値も変動するために、血液検査により重症度を客観的に数値化して評価することができます。
IgE
前述の「アトピー素因」で述べましたが、アトピー性皮膚炎では様々な物質に対してIgE抗体と呼ばれる即時型アレルギー(I型アレルギー)に関係する抗体を産生しやすく、血液検査でも様々な項目でIgE値(抗原特異的IgE値)が高くなる傾向があります。
(「アレルギーについて(総論)」の「”アレルギー”の検査法について」のページも参照)
血清IgE値は長期的にはアトピー性皮膚炎の病勢と相関することが知られていますが、かなりばらつきがあり、短期的な重症度のマーカーとしては有用ではありません。
★血清TARC値や血清IgE値測定によるアレルギー検査はいずれも保険適用となっています。アレルギー検査については、36項目が一度に測定できるMAST36をお勧めしています。
アトピー性皮膚炎の治療法ですが、近年は様々な治療法が存在し、選択の幅も広がっています。クリニックでの治療もそのほとんどをカバーしているため、重症度によらず対応できると考えます。(一部の内服薬は事前検査の関係で、クリニックで行いにくいものもあります)
ここでは、治療法の各論に入る前に、少し最近(2024年現在)のアトピー性皮膚炎の治療の進展と変遷について述べさせていただきます。
近年、アトピー性皮膚炎の病態の解明が進んできたことにより、治療も変化しつつあります。
ここ数年の間でも、新規の外用剤、内服薬、注射製剤などが多数発売、適応となり、今後も増加していくことが予想されます。
■アトピー性皮膚炎の治療の進展と変遷
アトピー性皮膚炎を含む皮膚疾患大部分について言えることですが、皮膚の細胞が障害を受けたり、皮膚で炎症反応が起こっているので、治療の中心が皮膚に直接作用する外用剤であることは今も昔も変わりません。特にアトピー性皮膚炎のような皮膚表面で起こっている湿疹反応を抑えるためには、その炎症反応を抑えるステロイド外用剤が治療の中心となることは今の時代も同じです。
ステロイドはその効果が幅広く、様々な細胞の核内や細胞膜の受容体に作用して、プロスタグランジンをはじめとする炎症性物質や、各免疫担当細胞が放出する炎症性サイトカインを抑制するため、効果は高いものがあります。ただ、その作用が疾患特異的ではないために他の作用が副作用として現れる場合もあります。外用剤の場合は内服薬のような全身に作用する副作用はありませんが、皮膚に起こる局所的な副作用は出る可能性はあります。
(ステロイド外用剤について詳しくは、「ステロイド外用剤について」のページを参照ください。)
ステロイド外用剤とは異なる機序として初めて登場した外用剤は、1999年に承認されたT細胞の活性を抑制する「タクロリムス(プロトピック軟膏®)」です。
タクロリムスはT細胞から産生される各種サイトカインの転写因子であるT細胞活性化因子(NF-AT)を抑制することで様々なサイトカイン産生を抑制します。ステロイドのような局所的副作用はなくなりましたが、幅広い免疫抑制があるために、アトピー性皮膚炎に特異的 な薬剤ではありません。
その後、アトピー性皮虞炎の病態の解明が進み、アトピー性皮膚炎の病態形成に直接関与する炎症性サイトカインが特定されてきたために、これらの炎症性サイトカインの働きやシグナル伝達経路を阻害する治療薬の開発が進み、新たなアトピー性皮膚炎の治療薬として注目されています。(前述した、「アトピー性皮膚炎の病態生理」の模式図を参照)
2018年に本邦では初の抗体製剤となるType2サイトカインのIL-4とIL-13の受容体抗体注射 製剤である「デュピルマブ(デュピクセント®)」が発売されました。
これを皮切りに次々と新規の治療薬が発売となります。
2020年には世界初となるJAK-STATシグナル伝達経路を阻害する外用JAK阻害剤「デルゴシチニブ(コレクチム軟膏®)」が発売。
2021年には経口JAK阻害薬「バリシチニブ(オルミネント®)」、「ウパダシチニブ(リンヴォック®)」がアトピー性皮膚炎に適応追加、「アブロシチニブ(サイバインコ®)」が発売。
2022年にはIL-31の受容体抗体注射製剤「ネモリズマブ(ミチーガ®)」が発売。
2023年にはIL-13を直接無力化する抗IL-13抗体注射製剤「トラロキヌマブ(アドトラーザ®)」が発売。
2024年にはIL-13に結合することでIL-13が標的細胞の受容体に結合できなくする抗IL-13 抗体注射製剤「レブリキズマブ(イブグリース®)」が発売。
また、少し異なったアプローチをする薬剤もあります。Th2細胞を含む様々な免疫担当細胞からの炎症性サイトカイン産生の促進や抑制には細胞内のcAMPという物質の濃度が関わっており、cAMPの濃度が低下すると炎症性サイトカインの産生が亢進して、制御性T細胞(T Reg)を介した抗炎症性サイトカインの産生が弱まります。
このcAMPを分解する酵素がPDE4という物質で、アトピー性皮虞炎の患者では元々PDE4の 活性が高まっており、cAMPの濃度が低下しているため炎症反応が亢進しています。
このPDE4を阻害し、細胞内のcAMPの濃度を増加させることで炎症反応を抑制することができます。
2022年に外用薬としては本邦初となる外用PDE4阻害薬「ジファミラスト(モイゼルト軟膏®)」が発売されました。
このように、新規の治療薬が開発され、選択の幅が広がることはすばらしいことですが、これらの強力な治療効果のある注射薬や内服薬は基本的に重症のアトピー性皮膚炎のみに適応があることと、価格が非常に高額であるため誰もが気軽に開始できるものではないところは問題点でもあります。また、新規の外用剤については、ステロイド外用剤に取って代わるほどの効果まではありませんが、プロアクティブ療法や維持期に使用したり、小児に使用しやすいなど治療の選択肢は広がります。副作用がほとんどないことも大きなメリットです。
以上のように、アトピー性皮膚炎の治療はステロイド外用剤が中心であることは変わらないと思われますが、その他の治療については現在過渡期であり、今後も発展していくと考えられます。
■当院における治療について
まず、アトピー性皮膚炎の治療の目標ですが、もともと皮膚が弱いところに原因がありますので、完全に根治させるということは難しいところがあります。ただ、適切な治療を行い、普段の日常生活でも悪化因子をできるだけ取り除くことで、皮膚の炎症が少しずつよくなり、最小限の薬で症状が落ち着いた状態を維持することができるようになります。
そのため、治療の目標として次のように設定します。

という状態をめざします。
アトピー性皮膚炎の治療は、病気そのものを完治させる薬はないことから、

の3つの方法を中心に行います。以下、それぞれについて詳しく説明していきます。

![]()
■ステロイド外用剤
症状が強い部位にはステロイド外用剤が最も効果があります。ステロイド外用剤には弱いものから強いものまで5段階に分類されており、皮疹の重症度や部位によって塗る薬のランクが変わってきます。ステロイド外用剤についてはその副作用を心配される患者様もいらっしゃると思いますが、正しい使い方をしていれば問題はありません。当院ではその点には十分 配慮して、塗り方や回数についてもしっかり説明しております。
ステロイド外用剤についてくわしく知りたい方は、「ステロイド外用剤について」をご覧ください。
■非ステロイド性免疫抑制外用剤
ある程度炎症が落ち着いた中等度以下の症状に適応があり、顔面や首回りによく使用されますが、ステロイド外用剤とのコンビネーションや、プロアクティブ療法の維持期にも使用します。メリットは長期間の使用の際に、ステロイド外用剤にみられる局所的な副作用がほとんどないことですが、炎症の強い部位に対しては効果が弱いと思われます。
最も歴史のあるものとして、T細胞の活性を抑制するタクロリムス軟膏(プロトビック軟膏® )があります。特徴としては分子量が大きく皮膚のバリア機能が破壊された悪い部位からしか吸収されないことが挙げられます。使用初期に刺激感が出ることがありますが、通常使用 を継続していると消退していきます。
その他、新規のものとしてJAK阻害外用薬であるデルゴシチニブ軟膏(コレクチム軟膏®)や、炎症性サイトカインの産生を抑えるPDE4阻害外用薬であるジファミラスト軟膏(モイゼルト軟膏®)があります。
★プロアクティブ療法について
ステロイド外用と非ステロイド外用のコンビネーション療法(下図)によりステロイド外用剤の使用量を少なくしたり、症状が良くなった後にも定期的・間欠的にステロイド外用や 非ステロイド外用を週に2、3回継続して行うことで再発予防を目的とするプロアクティブ療法(下図)が推奨されています。
皮膚症状が見た目にはよくなったとしても、皮内の炎症細胞浸潤はまだ残存している場合が多く、すぐに再発してくる可能性が高いからです。プロアクティブ療法を行うことで、局所的副作用を最小限に抑えつつ、再発を防ぎ、良い皮膚状態を保つことを目指します。
(これに対して、症状が改善したらステロイド外用を完全に断ち切って、保湿剤のみに変更して、また再燃してきたらステロイド外用を再開する方法をリアクティブ療法と言います。)
![]()
■抗ヒスタミン薬・抗アレルギー薬
皮疹を軽快させるのは外用剤ですが、かゆみが強いと引っ掻いてまた悪化させてしまうことがよくあります(Itch-scratch サイクル)。かゆみの程度は患者さんの感じ方などによっても違いますが、いずれにしてもかゆみを減らすことは大切な治療の一つです。
かゆみがひどくてイライラしたり、十分に眠れない時などは、かゆみを抑える目的で用いることがあります。ただし、かゆみを消退させるほどの強い効果はありません。
■ステロイド内服
皮膚病変の急性増悪時などに有効ですが、全身的副作用を考慮して、できるだけ短期間の投与にとどめます。(ガイドラインでは推奨されていません。)
■シクロスポリン内服
強力な免疫抑制剤で、ステロイド外用やタクロリムス外用を継続しても症状が改善しないような成人の重症患者が適応となります。皮膚症状の改善、かゆみの軽減に対する効果はとても高いですが、血圧上昇や腎機能障害などの副作用があり、1回の治療期間として最大12週 間までの投与が認められています。
■経口JAK阻害薬
アトピー性皮膚炎の病態形成に関わる炎症性サイトカインの標的細胞内でのシグナル伝達経路である「JAK-STATシグナル伝達経路」を阻害する薬剤です。
強力な抗炎症作用があり、ステロイド外用やタクロリムス外用を継続しても症状が改善しないような重症患者が適応となります。効果はとても高いですが、高額な薬剤であることと、 定期的な血液検査と胸部レントゲン検査が必要となります。
クリニックで処方する場合は、外部での胸部レントゲン検査の結果の提出が必要となります。
![]()
近年開発が進んでいる生物学的製剤と称される抗体注射薬です。現在(2023年)、4種類の製剤が発売されており、いずれも高い治療効果が期待できます。副作用が少なく、事前検査に胸部レントゲン検査が必要ないため、クリニックでの施行や処方も増加しています。
■デュピルマブ(デュピクセント®)
2018年に発売された本邦初の抗体製剤であり、炎症性サイトカインIL-4とIL-13の受容体の共通ユニットであるIL-4受容体αサブユニット対する抗体注射薬です。
IL-4とIL-13はアトピー性皮膚炎の病態形成に深く関わる炎症性サイトカインであり、その両方を抑制することで強力な抗炎症効果を発揮します。
他治療を継続しても症状が改善しない生後6ヵ月以上の重症患者が適応となります。
投与スケジュールに従って皮下注射しますが、自宅での自己注射も可能となっています。
高額な薬剤のため、診察をして適応がある場合に予約をしてからの発注となります。
■ネモリズマブ(ミチーガ®)
2022年に発売された炎症性サイトカインIL-31の受容体に対する抗体注射薬です。
IL-31は主にアトピー性皮膚炎におけるかゆみの誘発に深く関わる炎症性サイトカインであり、これを抑制することで強力なかゆみ抑制効果を発揮します。
他治療によるかゆみ抑制のコントロールができない6歳以上の重症患者が適応となります。
投与スケジュールに従って皮下注射しますが、自宅での自己注射も可能となっています。
高額な薬剤のため、診察をして適応がある場合に予約をしてからの発注となります。
■トラロキヌマブ(アドトラーザ®)
2023年に発売された炎症性サイトカインIL-13に結合して直接中和する抗体注射薬です。
IL-13はアトピー性皮膚炎の病態形成に深く関わる炎症性サイトカインですが、本薬剤の特徴として、IL-13に結合して直接無力化することで強力な抗炎症効果を発揮します。
他治療を継続しても症状が改善しない15歳以上の重症患者が適応となります。
投与スケジュールに従って皮下注射しますが、自宅での自己注射も可能となっています。
高額な薬剤のため、診察をして適応がある場合に予約をしてからの発注となります。
■レブリキズマブ(イブグリース®)
2024年に発売された炎症性サイトカインIL-13に結合することで、IL-13が受容体に結合することを阻害する抗体注射薬です。
IL-13はアトピー性皮膚炎の病態形成に深く関わる炎症性サイトカインであり、これを抑制することで強力な抗炎症効果を発揮します。
他治療を継続しても症状が改善しない12歳以上(体重40kg以上)の重症患者が適応となります。
投与スケジュールに従って皮下注射しますが、自宅での自己注射はまだできません。
高額な薬剤のため、診察をして適応がある場合に予約をしてからの発注となります。
![]()
■エキシマライト照射
紫外線のUVBを照射する光線治療は、従来よりアトピー性皮膚炎の付加的治療法として有効性が確認されており、保険適応にもなっています。特に、ステロイド外用剤に反応しにくい 場合や、かゆみの強い病変部や痒疹結節の部位に効果的です。当院ではUVBの中でも308nmの波長をもつ「エキシマライト」の照射を行っております。詳しくは「光線療法について」のページをご参照ください。

アトピー性皮膚炎の患者さんは皮膚のバリア機能が弱く、保湿成分が欠乏しているために乾燥肌であり、抗原(異物)や微生物などが侵入しやすく、これらは炎症を起こす原因になります。スキンケアによって皮膚が健康な状態に保たれると、さまざまな悪化因子の影響を受けにくくなり、発症の予防や悪化の回避につながります。スキンケアの基本は皮膚を清潔に保つことと、乾燥を防ぐために保湿剤を塗ることです。
まず、皮膚を清潔に保つために毎日の入浴・シャワーが重要です。シャンプー・石鹸は低刺激、敏感肌用を用いて、洗浄力の強いものは避ける必要があります。汗や汚れは強くこすらないようにして速やかにおとします。シャンプー・石鹸は残らないように十分にすすぎます。高い温度のお湯につかったり、入浴剤は避けるほうがよいかと思います。
また、保湿剤ですが入浴後はなるべく早めに必ず塗ります。また、何回塗っても問題ありませんので、少しかさついてきたと思ったら、また塗りなおします。軽い炎症のみなら保湿剤で治ってしまうこともあります。

「アトピー性皮膚炎の病因とは?」の欄にも書きましたが、病態形成の要因の1つに「皮膚バリア機能の低下」があります。アトピー性皮膚炎の患者様は通常よりも外的な刺激やアレルゲンに対して影響を受けやすくなっています。
日常の生活環境の中に悪化因子となるものはたくさんあります。すべてを除去することは 困難と思われますので、「できる限りで気をつける」というスタイルが大事だと思います。
例えば、室内環境ではこまめに掃除し、ダニやほこりの発生を少なくする環境を整えることが大切です。また、ダニの発生しやすいじゅうたんや布製の家具などはできるだけ避け、寝具類の取り扱いにも注意が必要です。また、室内は風通しをよくして、適温、適湿を保つようにすることも重要です。汗をなるべくかかないように、できるだけ涼しい環境づくりを心がけます。夏は適宜冷房を使用し、冬は暖房をきかせすぎないようにします。また、ペットを飼うこともできればやめておくほうが無難です。
外出時には、日焼けをしないように強い紫外線を避けたり、花粉や砂やほこりの多い環境はなるべく避ける必要があります。汗をかいた場合は早めにふきとり、帰宅時にはアレルゲン となりえる物質を家の中に持ち込まないように注意して、早めにシャワーを浴びたり、入浴して清潔を保つことが重要です。
また、衣類の材質にも気を配る必要があります。木綿素材などの肌触りのよい衣類を着用する必要があります。
洗濯の際は、洗剤のすすぎ残しがないように、すすぎをしっかり行うことが大切です。
また、心理的ストレスは重要な悪化因子の一つと考えられています。環境の変化、クラスがえ、試験、家族や友達、周囲の人との人間関係のトラブルなどで心理的ストレスがたまる と、それに反応してホルモンが分泌され、アレルギー反応を起こしやすくなると考えられています。なるべくストレスをためないように、自分なりのストレス解消法を身につけることが大切です。また、規則正しい生活、睡眠時間をしっかりとる、疲れた時は休養するといった生活習慣を心がけましょう。





















